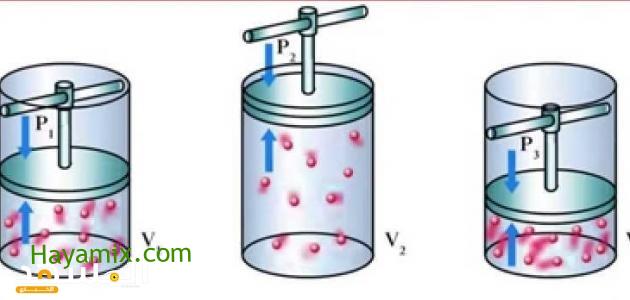
يتناسب حجم كمية معينة من الغاز عكسياً مع الضغط المطبق عليه عندما تكون درجة حرارته ثابتة. إلى ماذا يشير النص أعلاه؟ يعرّف قانون بويل أنه أحد قوانين الغاز التي تم بموجبها وضع قوانين الغاز المثالي ، وهذا القانون ينص على أن حجم كمية معينة من الغاز يتناسب عكسًا مع الضغط المطبق عليه إذا كانت درجة الحرارة ثابتة ، ومن خلال ذلك يمكننا استنتاج الإجابة على السؤال الصحيح. مع الضغط عليه عندما تكون درجة حرارته مستقرة.
يتناسب حجم كمية معينة من الغاز عكسياً مع الضغط المطبق عليه عندما تكون درجة حرارته ثابتة.
الإجابة الصحيحة على السؤال: يتناسب حجم كمية معينة من الغاز عكسياً مع الضغط الواقع عليه عندما تكون درجة حرارته ثابتة. هو أن البيان السابق يشير إلى قانون بويل.
قانون بويل
قام العالم روبرت بويل بتثبيت درجة حرارة الغاز (T) ثم قاس التغير الذي حدث في حجم الغاز (V) بعد تغيير ضغطه (P). يقل حجم الغاز عندما ينخفض الضغط عليه ويقل حجم الغاز عندما يزداد الضغط.
أي إذا زاد الضغط ، ينخفض الحجم بنفس النسبة ، وفي حالة زيادة الحجم ، ينخفض الضغط ، مع الحفاظ على نفس درجة الحرارة.
الخامس = 1 / ف
